수용체 차별화로 효능·안전성 개선 전망
한미 독자 플랫폼 기술 ‘랩스커버리’ 적용
효능·안전성·지속성 등 극대화
면역관문 억제제 병용요법 시 효능↑
한미약품은 미국 식품의약국(FDA)에 면역조절 항암 혁신신약 ‘HM16390(랩스인터루킨-2아날로그, LAPSIL-2analog)’ 임상 1상 시험계획(IND)을 신청했다고 3일 밝혔다. 진행성 또는 전이성 고형암 환자를 대상으로 안전성과 내약성, 약동학, 약력학 등을 평가하기 위한 임상으로 설계됐다.
HM16390은 면역세포 분화와 증식을 통해 면역 기능을 조절하는 것으로 알려진 인터루킨-2(IL-2)를 차별화해 새롭게 디자인한 IL-2 변이체다. 한미약품 독자 플랫폼 기술인 랩스커버리를 적용해 효능과 안전성, 지속성 등을 극대화한 면역조절 항암 혁신신약 후보물질이다.
항암 약물 치료 주기당 1회 피하 투여가 가능한 지속형 제제로 기존 IL-2 제제와 차별화된 수용체 결합력을 통해 항암 효능을 크게 향상시켰다고 한미약품 측은 설명했다. 흑색종과 대장암뿐 아니라 신장암과 췌장선암의 동물모델 등에서 우수한 효능을 확인했다. 이를 바탕으로 다양한 진행성 또는 전이성 고형암에서 치료 효능을 발휘할 것으로 기대하고 있다.
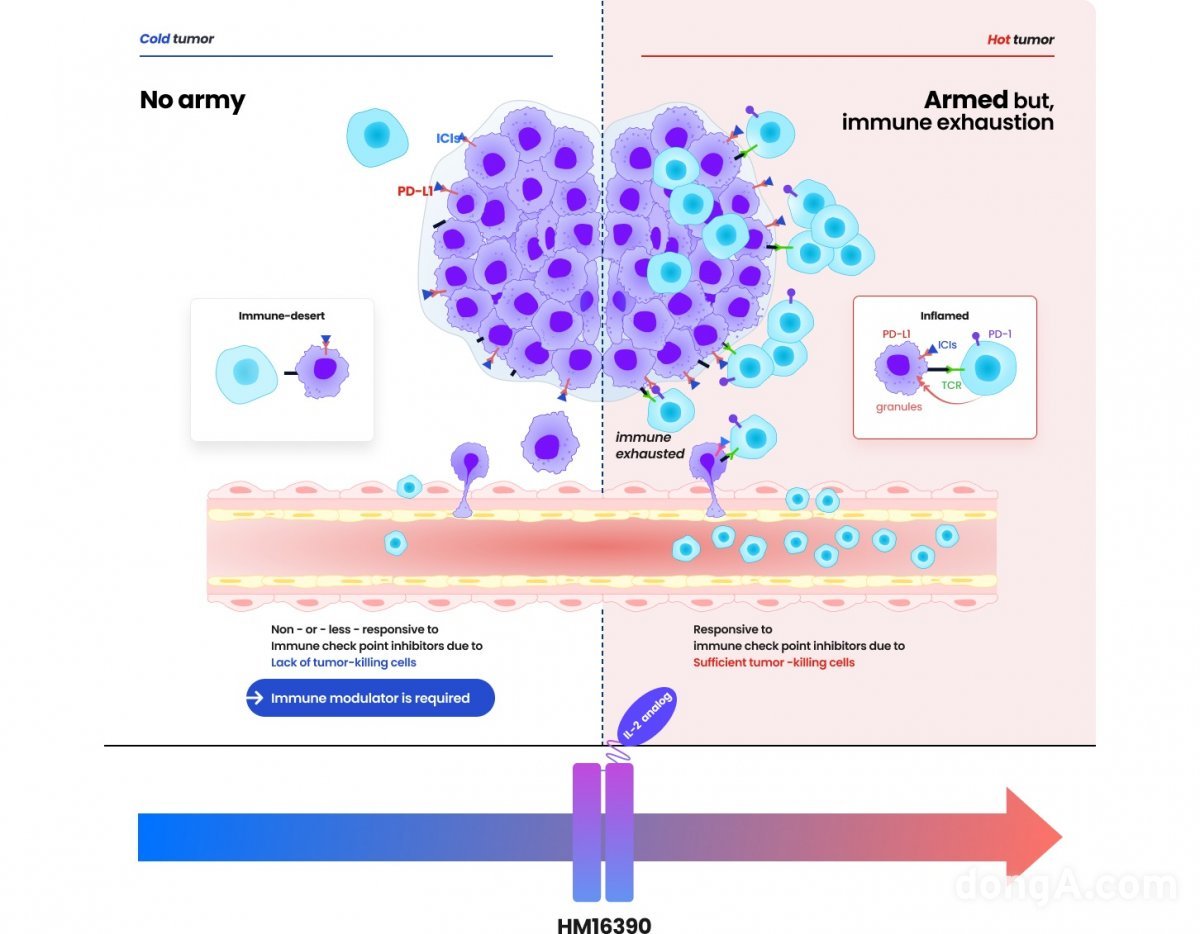
한미약품의 경우 HM16390은 우수한 항종양 효능을 발휘하면서 안전성을 대폭 개선해 단독요법 효과도 기대할 수 있고 전 세계적인 추세에 맞춰 면역관문 억제제와 병용 시 치료 효과를 끌어올릴 수 있을 것으로 보고 있다. 또한 면역관문 억제제에 반응을 보이지 않는 ‘차가운 종양(cold tumor)’에서도 치료 효과를 이끌어낼 수 있는 중요한 치료 옵션이 될 것으로 예상된다.
한미약품 관계자는 “항종양 효능 극대화와 함께 안전성까지 개선된 HM16390은 단독요법은 물론 면역관문 억제제 병용 시 종양미세환경을 변화시켜 치료 효과를 크게 높일 수 있을 것으로 기대하고 있다”며 “기존 치료제에 반응하지 않는 암 환자에게 대안이 되는 차세대 면역조절 항암제 개발을 완수할 수 있도록 임상과 연구에 더욱 매진하겠다”고 강조했다.
HM16390은 지난 2022년 9월 국가신약개발 과제로도 선정된 바 있다. 국가신약개발사업은 정부가 미충족 의료 수요가 높은 분야 치료제 개발을 촉진하기 위해 제약바이오 기업과 학교, 연구소, 병원 등의 신약개발을 지원하는 국가 R&D 지원 제도다.
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개



댓글 0