그러나 임상시험은 절대 시험삼아 대충 하는 게 아니다. 임상시험은 국제적인 규약에 따라 허가를 받은 의료진이 엄격하고 까다로운 절차 속에서 진행한다.
특히 지푸라기라도 잡고 싶은 암 환자에게 임상시험은 한 줄기 희망이지만 그렇다고 누구나 임상시험에 참여할 수 있는 것은 아니다.
특정한 약의 임상시험에 대상자의 몇십배나 되는 환자가 몰려 애원하는 일은 흔하다. 그러나 임상시험이 무엇인지, 한계는 무엇인지에 대해 아는 사람은 드물다.
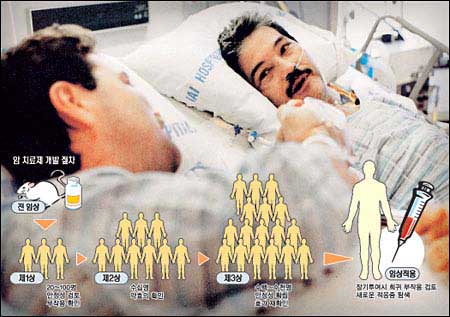
▽임상시험이란?〓임상시험은 신약(新藥) 개발의 필수적이고 최종적인 과정이다. 제약회사는 약이 될 만한 후보 물질을 찾아내면 우선 실험실에서 세포나 조직의 차원에서 항암 효과를 테스트한다. 다음으로 동물을 대상으로 독성은 없는지, 투여 뒤 어느 정도 약효가 지속되는지, 어떤 형태의 약이 가장 효과적인지 등을 검사한다. 이 모든 단계를 거쳐 마지막으로 사람을 대상으로 약의 안전성과 효과를 검증하는 것이 바로 임상시험이다.
▽임상시험의 절차〓임상시험을 수행할 의사는 자신이 속한 의료기관의 ‘임상시험 심사위원회’(IRB) 또는 윤리위원회로부터, 제약회사는 식품의약품안전청으로부터 각각 임상시험 허가를 받아야 시작할 수 있다.
일반적으로 3단계에 걸친 임상시험 결과 끝에 시판 허가가 나오지만 암이나 에이즈, 희귀질환은 2차 임상시험 뒤 시판허가를 얻은 상태에서 3차 임상시험을 진행한다. 따라서 일반 약은 임상시험이 최소 5, 6년이 걸리지만 암 치료제는 빠르면 3년 만에도 허가를 얻을 수 있다.
암의 경우 1단계 임상시험에서는 몇 달 동안 여러 종류의 암환자 20∼100명을 대상으로 효과, 적절한 용량, 부작용 등을 측정한다. 2단계 임상 때에는 몇 달에서 2년 정도까지 특정 암 환자 몇십명을 대상으로 항암 효과를 관찰한다. 치료제를 투여했을 때 암세포가 어느 정도 없어지는지를 꼼꼼히 보며 보통 종양 크기가 절반 정도로 줄어들었을 때 ‘반응이 있다’고 한다.
3단계 임상은 수백명에서 수천명을 대상으로 기존의 치료제와 비교하며 효과와 부작용, 경제적 이점 등을 보기 때문에 수 년이 걸리는 경우가 많다. 보통은 두 그룹으로 나눠 한쪽에는 새 치료제를 투여하고, 다른 한쪽에는 기존의 치료제를 투여해서 비교한다. 기존의 치료제가 전혀 없는 경우에는 위약(僞藥)을 투여해서 비교한다.
▼국내 임상시험중인 항암제▼
| 제품 | 구분 | 제약회사 | 대상 암 | 단계 |
| DA-125 | 주사제 | 동아제약 | 항암제에 반응이 없거나 재발한 급성백혈병 | 1상 |
| 제넥솔 | 〃 | 삼양사 | 비(非)소세포폐암 | 2상 |
| 제넥솔-PM | 〃 | 〃 | 각종암 | 1상 |
| 선플라 | 〃 | SK제약 | 진행성 위암 | 2, 3상 |
| 두경부 상피세포암 | 1, 2상 | |||
| CKD-602 | 〃 | 종근당 | 진행성 위암, 소세포폐암, 항암제 플라티늄이 듣지 않는 진행성 난소암, 진행성 대장암 | 2상 |
| 젤로다 | 정제 | 한국로슈 | 진행성 또는 전이성 위암 | 2상 |
| 탁소텔 | 주사제 | 아벤티스 파마 | 일부 유방암, 국소적으로 진행된 재발성 및 전이성 비(非)소세포폐암 | 3상 |
| 항암제 치료를 받지 않은 전이성 또는 국소재발성 위암 | 2상 | |||
| 알림타 | 〃 | 한국릴리 | 항암제 치료를 받았던 국소 진행성 또는 전이성 비(非)소세포폐암(환자 등록 완료) | 3상 |
| 젬자 | 〃 | 한국릴리 | 국소적으로 진행되거나 전이된 비소세포폐암 | 3상 |
| 수술가능한 비소세포폐암 | 2상 |
▽임상시험을 받으려면?〓임상시험은 더 이상 치료방법이 없거나 기존의 치료법이 잘 듣지 않을 경우 좀더 나은 치료 ‘가능성’을 기대하며 받는 것이 원칙이다.
암 환자들은 언론 등을 통해 새 약 소식을 들으면 한꺼번에 몰려든다. 지난해 폐암 치료제 이레사 소동이 대표적인 예이다. 그러나 지난해 초 국내에서 선보인 ‘글리벡’이 세계적으로 엄청난 주목을 받았던 것과 달리 외국에서는 이레사가 임상시험 중인 여러 약 중의 하나일 따름이다.
더러 기존의 치료법이 잘 듣는데도 이를 포기하고 임상시험을 받는 경우가 있다. 이 경우 자칫 치료 시기를 놓쳐 오히려 환자에 해가 되기도 한다. 가능하면 주치의와 상담해서 득실을 따져 임상시험 참가를 결정해야 한다.
국내에서는 10여개의 항암제가 임상시험 중이지만 세계적으로는 수 백개를 헤아린다. 미국 국립암연구소는 인터넷 홈페이지(www.cancer.gov)를 통해 임상시험을 받을 수 있는 방법, 병원 등을 자세히 알려주고 있다.
이성주 기자 stein33@donga.com
▼GCP
Good Clinical Practice의 준말로 ‘임상시험 관리 기준’으로 번역된다. 임상시험을 받는 환자의 권리를 보호하고 시험 결과의 신뢰성을 확보하기 위한 법적 기준을 뜻한다. 1981년 미국이 처음으로 GCP를 만들었으며 일본은 90년, 우리나라에서는 95년 10월 법제화했다. 97년 국제적 기준이 만들어져 각국의 임상시험 기준이 통일화되고 있으며 우리나라도 지난해 1월 이 기준에 맞춰 임상시험을 진행토록 하고 있다.
인구 고령화 : 인구 고령화 원인 : 수명 연장으로 노령 인구 증가 >
-

경제 Inside Out
구독
-

오늘과 내일
구독
-

횡설수설
구독
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개
-
- 추천해요
- 개

![전세 계약 전 근저당권 반드시 확인하세요[부동산 빨간펜]](https://dimg.donga.com/a/464/260/95/1/wps/NEWS/FEED/Donga_Home_News/130480037.1.thumb.jpg)

