대웅제약, 당뇨병 치료제 혁신신약 임상 3상 본격화… 단독·병용 시험 동시 승인
- 동아경제
-
입력 2020년 10월 6일 17시 42분
공유하기
글자크기 설정
대웅제약 이나보글리플로진 임상 3상 승인
환자 총 230여명 규모 단독·병용 요법 임상 진행
오는 2023년 국내 발매 목표

대웅제약이 당뇨병 치료 혁신신약 후보물질에 대한 임상 3상을 본격화한다.
대웅제약이 당뇨병 혁신신약 후보물질에 대한 단독 및 병용 사용 관련 임상 3상에 돌입한다.
대웅제약은 SGLT-2 수용체 억제제 신약인 ‘이나보글리플로진’의 단독요법과 메트포르민(Metformin) 병용 요법 각각에 대한 유효성과 안전성을 평가하는 3상 임상시험을 식품의약품안전처로부터 동시에 승인 받았다고 6일 밝혔다.
이나보글리플로진은 콩팥에서 포도당 재흡수에 관여하는 SGLT-2 수용체를 선택적으로 억제해 포도당을 직접 소변으로 배출시키는 기전의 의약품으로 개발이 추진되고 있다. 지난 9월 국제학술대회 ‘2020 ICDM’에서 성공적인 임상 2상 결과를 처음 공개한 바 있다.
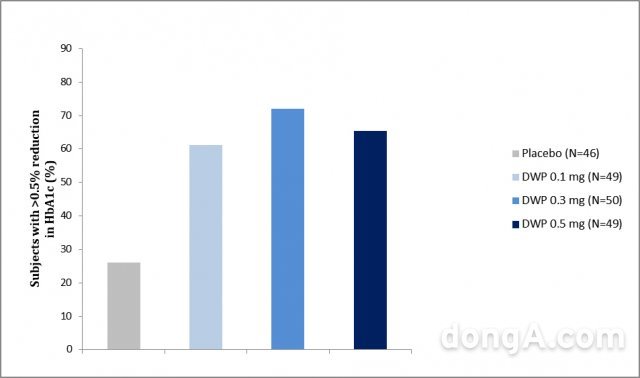
또한 국제적인 당뇨병 조절목표인 ‘당화혈색소 7.0% 이하로 도달한 환자 비율’이 최대 61%에 달해 기존 SGLT-2 억제제보다 20% 이상 좋은 결과를 보였고 치료 전 대비 당화혈색소 0.5% 초과 감소한 환자비율은 동일 계열 약물의 40~60% 수준 대비 최대 72%를 기록해 탁월한 혈당감소 효과를 추가로 입증했다고 밝혔다.
전승호 대웅제약 사장은 “대웅제약은 SGLT-2 당뇨병 신약인 ‘이나보글리플로진’이 계열 내 최고신약(베스트 인 클래스, BEST IN CLASS)으로 자리매김할 수 있도록 연구·개발에 역량을 집중할 계획”이라며 “국내는 물론 글로벌 시장을 목표로 이나보글리플로진을 제2형 당뇨병 환자들에게 좋은 치료옵션으로 제공할 수 있도록 힘쓸 것”이라고 말했다.
동아닷컴 김민범 기자 mbkim@donga.com
트렌드뉴스
-
1
대낮 하늘서 굉음…7t짜리 불덩어리가 떨어졌다
-
2
李 “기간제 2년 되면 정규직 전환, 말은 좋은데 되레 장애”
-
3
57세에 치매 환자 된 내과 의사 “답은 ‘조기 진단’ 강화”[노화설계]
-
4
이부진 주총 패션 ‘구찌 재킷에 발렌티노 시스루’…가방은 에르메스
-
5
대만 ‘南韓’ 보복 표기에…中 “한국은 ‘하나의 중국’ 견지할거라 믿어”
-
6
[단독]“기장 살해 前부기장, 메디컬 테스트 떨어져…비행 못하자 퇴사”
-
7
광화문은 이미 ‘아미 로드’…“BTS 보이는 모든 곳이 포토존”
-
8
한국 ‘석달 방출량’ 맞먹는 원유 확보… 인도-日-EU도 뛰어들어
-
9
[단독]BTS, 뉴욕 브루클린 브릿지 상공서 드론쇼로 컴백 포문 열었다
-
10
가방에 맞은 머리 극심통증…병원가니 “뇌종양입니다”
-
1
[송평인 칼럼]한 사람을 위한 사법 변경
-
2
주호영 “호남출신, 대구 만만히 봐” 이정현 “꿩-알 먹고 털도 탐내”
-
3
[사설]“우린 공소청장이라 부르면 돼”… 與 대표의 어깃장
-
4
김어준 유튜브 나간 한준호, ‘거래설’-정청래 때렸다
-
5
가스전 폭격당한 이란, 카타르 ‘LNG 심장’ 보복 공격
-
6
주호영 “이정현, 지선 장애물…이진숙 전략공천? 대구시민 무시”
-
7
李 “고용유연성, 노동자 일방적 희생 옳지 않아”
-
8
美, 하르그섬 지상군 투입? 해병대 2500명 탄 상륙함, 日서 중동 이동
-
9
“AI가 초급 개발자 대체 비상상황” 일자리 직격탄 맞은 청년들
-
10
하투하 ‘강강술래 경호’ 눈총…“인천공항 입구 독차지”
트렌드뉴스
-
1
대낮 하늘서 굉음…7t짜리 불덩어리가 떨어졌다
-
2
李 “기간제 2년 되면 정규직 전환, 말은 좋은데 되레 장애”
-
3
57세에 치매 환자 된 내과 의사 “답은 ‘조기 진단’ 강화”[노화설계]
-
4
이부진 주총 패션 ‘구찌 재킷에 발렌티노 시스루’…가방은 에르메스
-
5
대만 ‘南韓’ 보복 표기에…中 “한국은 ‘하나의 중국’ 견지할거라 믿어”
-
6
[단독]“기장 살해 前부기장, 메디컬 테스트 떨어져…비행 못하자 퇴사”
-
7
광화문은 이미 ‘아미 로드’…“BTS 보이는 모든 곳이 포토존”
-
8
한국 ‘석달 방출량’ 맞먹는 원유 확보… 인도-日-EU도 뛰어들어
-
9
[단독]BTS, 뉴욕 브루클린 브릿지 상공서 드론쇼로 컴백 포문 열었다
-
10
가방에 맞은 머리 극심통증…병원가니 “뇌종양입니다”
-
1
[송평인 칼럼]한 사람을 위한 사법 변경
-
2
주호영 “호남출신, 대구 만만히 봐” 이정현 “꿩-알 먹고 털도 탐내”
-
3
[사설]“우린 공소청장이라 부르면 돼”… 與 대표의 어깃장
-
4
김어준 유튜브 나간 한준호, ‘거래설’-정청래 때렸다
-
5
가스전 폭격당한 이란, 카타르 ‘LNG 심장’ 보복 공격
-
6
주호영 “이정현, 지선 장애물…이진숙 전략공천? 대구시민 무시”
-
7
李 “고용유연성, 노동자 일방적 희생 옳지 않아”
-
8
美, 하르그섬 지상군 투입? 해병대 2500명 탄 상륙함, 日서 중동 이동
-
9
“AI가 초급 개발자 대체 비상상황” 일자리 직격탄 맞은 청년들
-
10
하투하 ‘강강술래 경호’ 눈총…“인천공항 입구 독차지”
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개



댓글 0